In het vorige werkblad heb je gezien hoe een gas zich gedraagt in een zuiger waarbinnen wordt voldaan aan de wet van behoud van energie. In dat geval geldt , waarbij een exponent is die wordt bepaald door de vrijheidsgraden van het gas - in onze simulatie werken we met mono-atomaire gassen in 2D.
We hadden kunnen denken dat we de ideale gaswet zouden kunnen gebruiken. Echter, de temperatuur van het gas verandert door de werking van de zuiger - deze verricht arbeid.
Het meenemen van arbeid dat verricht wordt door, of op, het gas is een eerste uitbreiding die belangrijk is in Thermodynamica. Uitwisseling van energie (toevoegen of afvoeren van warmte) is een tweede uitbreiding. In deze simulatie onderzoeken we die uitbreiding waarbij we warmte aan en af voeren uit het controlevolume. Op die manier kunnen we ook isotherme simulaties doen.
Eerst herhalen we de nodige ingrediënten:
klasse voor het deeltje met bijbehorende functies
variabelen en randcondities van controle volume
functies voor een lijst deeltjes
Daarna voegen we de code toe voor het warmtecontact:
introduceren thermostaat
En vervolgens
bestuderen isotherm proces
Laden van eerdere code¶
De pakketten van Python en de constanten voor de simulatie:
import numpy as np
import matplotlib.pyplot as plt
from matplotlib.animation import FuncAnimation
from scipy.optimize import curve_fit
BOX_SIZE_0 = 1e-8 # Hoogte en lengte startvolume (0.1 uM)
N = 40 # Aantal deeltjes in (0.1 uM)^3
V_0 = 400 # Startsnelheid van deeltjes
RADIUS = 1e-10 # Straal van moleculen
DT = 7.5e-14 # Tijdstap om geen botsing te missen
V_PISTON_0 = -0.1 * V_0 # Beginsnelheid van de zuiger
k_B = 1.38E-23 # Boltzmann constante
# (negatief betekent zowel links als rechts naar binnen gericht)De klasse voor het gasmolecuul met de interacties:
class ParticleClass:
def __init__(self, m, v, r, R):
""" maakt een deeltje (constructor) """
self.m = m
self.v = np.array(v, dtype=float)
self.r = np.array(r, dtype=float)
self.R = R
def update_position(self):
""" verandert positie voor één tijdstap """
self.r += self.v * DT
@property
def momentum(self):
return self.m * self.v
@property
def kin_energy(self):
return 1/2 * self.m * np.dot(self.v, self.v)
def collide_detection(p1: ParticleClass, p2: ParticleClass) -> bool:
""" Geeft TRUE als de deeltjes overlappen """
return np.linalg.norm(p1.r - p2.r) < (p1.R + p2.R)
def particle_collision(p1: ParticleClass, p2: ParticleClass):
""" past snelheden aan uitgaande van overlap """
m1, m2 = p1.m, p2.m
delta_r = p1.r - p2.r
delta_v = p1.v - p2.v
dot_product = np.dot(delta_r, delta_v)
# Als deeltjes van elkaar weg bewegen dan geen botsing
if dot_product >= 0: # '='-teken voorkomt ook problemen als delta_r == \vec{0}
return
distance_squared = np.dot(delta_r, delta_r)
# Botsing oplossen volgens elastische botsing in 2D
p1.v -= 2 * m2 / (m1 + m2) * dot_product / distance_squared * delta_r
p2.v += 2 * m1 / (m1 + m2) * dot_product / distance_squared * delta_rDe randvoorwaarde van het volume. Hierbij is rekening gehouden met een bewegende zuiger die in het vorige werkblad is toegevoegd.
def top_down_collision(particle: ParticleClass):
global impulse_outward, box_height
if abs(particle.r[1]) + particle.R > box_height / 2:
particle.r[1] = np.sign(particle.r[1]) * (box_height/2 - particle.R)
impulse_outward += abs(particle.momentum[1]) * 2
particle.v[1] *= -1
def left_right_collision(particle: ParticleClass):
""" verzorgen van botsingen met wand links en rechts, die als zuiger kunnen bewegen """
global box_length, v_piston, impulse_outward, work
if abs(particle.r[0]) + particle.R > box_length / 2:
particle.r[0] = np.sign(particle.r[0]) * (box_length/2 - particle.R)
piston_velocity = np.sign(particle.r[0]) * v_piston
relative_velocity = particle.v[0] - piston_velocity # stelsel zuiger
particle.v[0] = -relative_velocity + piston_velocity # stelsel waarnemer
impulse_outward += 2 * particle.m * abs(relative_velocity)
work += 2 * particle.m * relative_velocity * piston_velocityDe functies voor het uitvoeren van de functies over de gehele lijst met deeltjes, waarbij we de werking van de zuiger ook hebben meegenomen:
def create_particles(particles):
""" Leegmaken en opnieuw aanmaken van deeltjes in lijst """
global box_length, box_height
particles.clear()
for _ in range(N):
vx = np.random.uniform(-V_0, V_0)
vy = np.random.choice([-1, 1]) * np.sqrt(V_0**2 - vx**2)
x = np.random.uniform(-box_length/2 + RADIUS, box_length/2 - RADIUS)
y = np.random.uniform(-box_height/2 + RADIUS, box_height/2 - RADIUS)
particles.append(ParticleClass(m=1.0, v=[vx, vy], r=[x, y], R=RADIUS))
def temperature(particles) -> float:
"""Berekent de temperatuur van het gas uit de kinetische energie van alle deeltjes"""
total_kinetic_energy = sum(p.kin_energy for p in particles)
temp = total_kinetic_energy / (N * k_B) # 2D monoatomair gas: d/2 * k_B = k_B
return temp
def handle_collisions(particles):
""" alle onderlinge botsingen afhandelen voor deeltjes in lijst """
num_particles = len(particles)
for i in range(num_particles):
for j in range(i+1, num_particles):
if collide_detection(particles[i], particles[j]):
particle_collision(particles[i], particles[j])
def handle_walls(particles):
""" botsing met wanden controleren voor alle deeltjes in lijst en gemiddeld bepaling druk """
global pressure, impulse_outward, box_height, box_length # om pressure buiten de functie te kunnen gebruiken
impulse_outward = 0.0
for p in particles:
left_right_collision(p)
top_down_collision(p)
pressure = 0.95 * pressure + 0.05 * impulse_outward / ((2 * box_length + 2 * box_height) * DT)
def take_time_step(particles):
""" zet tijdstap voor een lijst deeltjes en verwerk alle botsingen onderling en met wanden """
global box_length, v_piston
box_length += 2 * v_piston * DT # zowel links als rechts zuiger
for p in particles:
p.update_position()
handle_collisions(particles)
handle_walls(particles)
Test code¶
Voordat we de code aanpassen controleren we eerst of alles het doet. Hiervoor maken we zowel een -diagram als een -diagram (met als toevoeging een -diagram) tijdens de werking van de zuiger. Let op! De eenheden van deze grafiek kunnen niet kloppen omdat er niet in verrekend zit welke constanten jij hebt gekozen.
particles = []
volumes = np.zeros(1000, dtype=float)
pressures = np.zeros(1000, dtype=float)
temperatures = np.zeros(1000, dtype=float)
# times = np.linspace(1, 100, 100)
pressure = 0.0
work = 0.0
box_height = BOX_SIZE_0
box_length = BOX_SIZE_0 # zetten zuiger terug
v_piston = V_PISTON_0
create_particles(particles) # resetten deeltjes
for i in range(1000):
take_time_step(particles)
volumes[i] = box_length * box_height
pressures[i] = pressure
temperatures[i] = temperature(particles)
fig, (ax1, ax2, ax3) = plt.subplots(1, 3, figsize=(12, 3))
ax1.set_xlabel('Volume')
ax1.set_ylabel('Pressure')
ax2.set_xlabel('Volume')
ax2.set_ylabel('Temperature')
ax3.set_xlabel('Pressure')
ax3.set_ylabel('Temperature')
fig.tight_layout
ax1.plot(volumes, pressures, '-r')
ax2.plot(volumes, temperatures, '-b')
ax3.plot(pressures, temperatures, 'r--')
plt.subplots_adjust(wspace=0.3) # afstand tussen subplots
plt.show()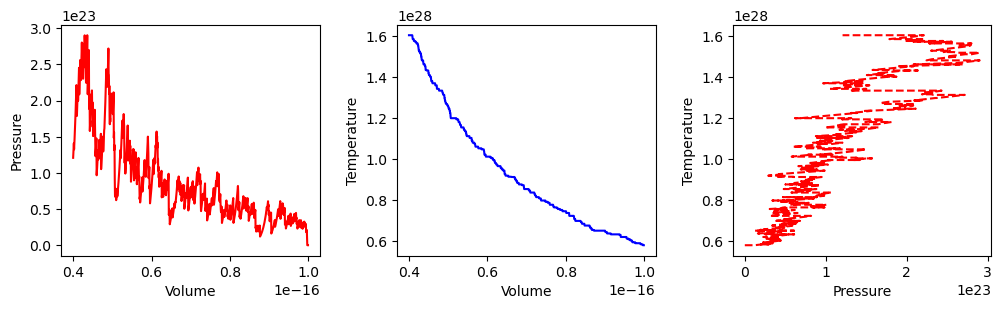
We zien inderdaad de druk, , met een exponent , wat verklaard wordt door de toename van de temperatuur tijdens het proces.
Maar wat gebeurt er wanneer we de temperatuur van het gas constant houden? Als we dat doen kunnen we controleren of de druk inderdaad invers proportioneel is met het volume, zoals de gaswet voorschrijft.
De thermostaat¶
In de werkelijkheid is de temperatuur van de wand een mate van de amplitude van de trillingen van de deeltjes waaruit de wand bestaat. De wederzijdse overdracht van de energie van die trillingen naar de kinetische energie van de gasmoleculen bepaalt het thermische contact tussen de wanden van het volume en het gas. In ons model bestaat de wand echter helemaal niet uit deeltjes maar hebben we een denkbeeldige lijn getrokken in de ruimte. We moeten daarom een wiskundige truc toepassen om de temperatuur van het gas te beïnvloeden.
Er zijn in de literatuur verschillende van dit soort trucs bedacht. Ze worden een ‘thermostaat’ genoemd. Elk van die type trucs hebben hun voor- en nadelen. In ons geval houden we het simpel: Op het moment dat een gasmolecuul botst met de wand (die een thermisch contact voorstelt), dan schalen we de snelheid van dit molecuul met (de wortel van) de verhouding tussen de veronderstelde temperatuur van de wand en de temperatuur die het gas op dat moment heeft:
Voor het gemak houden we de linker en rechter wand van het volume als zuiger en maken we het thermische contact aan de onder- en bovenwand.
def top_down_collision(particle: ParticleClass) -> None:
""" verzorgen van botsingen met wand boven en onder, die als thermostaat kunnen werken """
global box_height, set_temp, impulse_outward, heat
if abs(particle.r[1]) + particle.R > box_height / 2:
# Bereken de factor waarmee de snelheid moet worden geschaald
# om de temperatuur van het deeltje aan te passen naar de wandtemperatuur
temp_factor = (set_temp / temperature(particles)) if set_temp > 0 else 1.0
# Zet de positie van het deeltje terug binnen de box zodat het niet door de wand gaat
particle.r[1] = np.sign(particle.r[1]) * (box_height/2 - particle.R)
# Bereken de impuls die het deeltje naar buiten overbrengt bij de botsing
# en pas de impuls aan met de temperatuursfactor
impulse_outward += abs(particle.momentum[1]) * (1 + temp_factor**0.5)
# Houd bij hoeveel warmte er is overgedragen door deze botsing
# Positief betekent energie toegevoegd aan het deeltje, negatief betekent energie afgenomen van het deeltje
heat += particle.kin_energy * (temp_factor - 1)
# Schaal de snelheid van het deeltje zodat kinetische energie overeenkomt
# met de temperatuur van de wand (thermostaatwerking)
particle.v *= temp_factor**0.5
# Keer de verticale component van de snelheid om, zodat het deeltje terugkaatst
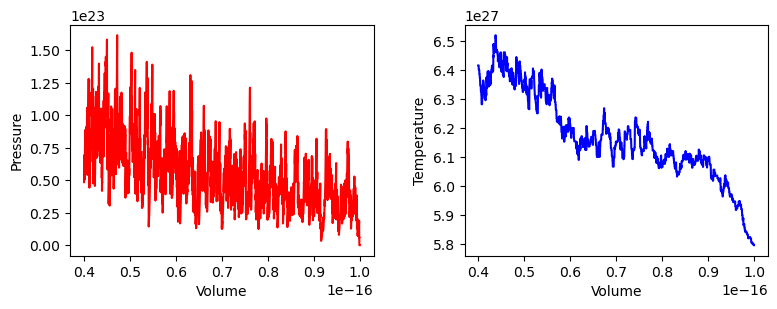
particle.v[1] *= -1Met deze nieuwe definitie van de functies, draaien we een simulatie waarin we zowel de temperatuur als de druk plotten als functie van het volume.
Om verdere belasting van de processor tot een minimum te beperken, berekent deze simulatie ook alvast de totale warmte en de totale arbeid tijdens het proces.
Deze worden opgeslagen in de arrays heats en works.
We zullen de resultaten van deze simulatie voor een aantal vervolgstappen gebruiken.
particles = []
N_steps = 5000
volumes = np.zeros(N_steps, dtype=float)
pressures = np.zeros(N_steps, dtype=float)
temperatures = np.zeros(N_steps, dtype=float)
heats = np.zeros(N_steps, dtype=float)
works = np.zeros(N_steps, dtype=float)
pressure = 0.0
work = 0.0
heat = 0.0
box_height = BOX_SIZE_0
box_length = BOX_SIZE_0 # zetten zuiger terug
v_piston = 0.2 * V_PISTON_0
create_particles(particles) # resetten deeltjes
set_temp = temperature(particles)
for i in range(N_steps):
take_time_step(particles)
volumes[i] = box_length * box_height
pressures[i] = pressure
temperatures[i] = temperature(particles)
heats[i] = heat
works[i] = work
if i%500==0:
print(i)
fig, (ax1, ax2) = plt.subplots(1, 2, figsize=(9, 3))
ax1.set_xlabel('Volume')
ax1.set_ylabel('Pressure')
ax2.set_xlabel('Volume')
ax2.set_ylabel('Temperature')
fig.tight_layout
ax1.plot(volumes, pressures, '-r')
ax2.plot(volumes, temperatures, '-b')
plt.subplots_adjust(wspace=0.3)
plt.show()0
500
1000
1500
2000
2500
3000
3500
4000
4500
Tip
Het zelfstandig afschatten van p0 is lastig, maar omdat de relatie tussen en bekend is, kunnen we wel een eerste stap maken door twee van onze metingen te nemen ( en en en ), delen we die waarden door elkaar en nemen we links en rechts de logaritme krijgen we:
Zo hebben we een schatting () voor gevonden. Door die waarde nu te substitueren vinden we een initiele guess () voor de waarde van :
Let op het - teken! Waar we nog verder rekening mee moeten houden is dat een verkeerde waarde voor kan zorgen voor hele grote fouten in omdat die exponentieel mee telt. Omdat en fluctueren door het gering aantal deeltjes kunnen we beter waarden voor sampelen waarbij we een keuze maken moeten tussen grotere sample size voor reduceren van ruis en kleine sampele size om het effect van de zuiger klein te houden:
p0 = np.mean(pressures[100:110])
p1 = np.mean(pressures[N:N+10])
V0 = np.mean(volumes[100:110])
V1 = np.mean(volumes[N:N+10])
n_init = -np.log(p0/p1) / np.log(V0/V1)
a_init = p0 * V0**(-n_init)p0 = np.mean(pressures[100:110])
p1 = np.mean(pressures[-10:])
V0 = np.mean(volumes[100:110])
V1 = np.mean(volumes[-10:])
n_init = -np.log(p0/p1) / np.log(V0/V1)
a_init = p0 * V0**(n_init)
print(n_init)
print(a_init)0.48160150709205923
741833226813209.9
def power_law(vol, a, n):
return a * vol**n
# Curve fit uitvoeren
params, covariance = curve_fit(power_law, volumes, pressures, p0=[a_init, n_init])
a_fit, n_fit = params
print(f"Fit resultaten: a = {a_fit:.3e}, n = {n_fit:.3f}")
# Plot simulatie en fit
plt.figure(figsize=(5,4))
plt.plot(volumes, pressures, '-r', label='Simulatie')
plt.plot(volumes, power_law(volumes, a_fit, n_fit), '--k', label=f'Fit: a={a_fit:.2e}, n={n_fit:.2f}')
plt.xlabel('Volume')
plt.ylabel('Pressure')
plt.legend()
plt.show()
Fit resultaten: a = 7.418e+14, n = 0.482
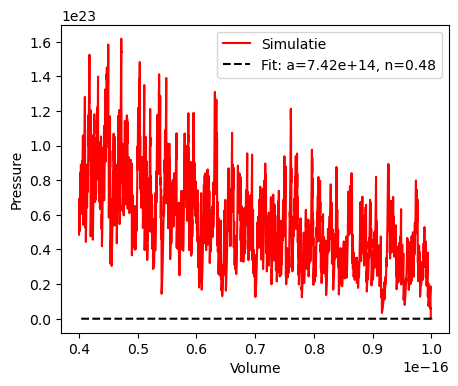
Je ziet dat de exponent van dit -diagram net niet overeenkomt met de ideale verwachting.
Als je goed kijkt zie je dat de temperatuur voor kleinere volumes een steeds grotere afwijking vertoont.
Al met al lijkt het resultaat van de simulatie er redelijk uit te zien. Maar om een sterkere indicatie te hebben dat de simulatie correct is, moeten we weer een goede test verzinnen om de simulatie te verifiëren. In dit geval kunnen we opnieuw controleren of de simulatie voldoet aan de eerste hoofdwet.
# arrays voor interne energie
internal_energy = np.zeros(N_steps)
# tijdens simulatie, al in je loop:
for i in range(N_steps):
take_time_step(particles)
volumes[i] = box_length * box_height
pressures[i] = pressure
temperatures[i] = temperature(particles)
heats[i] = heat
works[i] = work
# interne energie per stap
internal_energy[i] = np.sum([p.kin_energy for p in particles])
if i % 500 == 0:
print(i)
# Delta U t.o.v beginwaarde
delta_U = internal_energy - internal_energy[0]
# Controle eerste hoofdwet: Q - W
delta_QW = heats - works
# Plot
plt.figure(figsize=(6,4))
plt.plot(delta_U, label='ΔU (kinetische energie)')
plt.plot(delta_QW, '--', label='Q - W')
plt.xlabel('Tijdstap')
plt.ylabel('Energie')
plt.legend()
plt.title('Controle eerste hoofdwet')
plt.show()
plt.figure(figsize=(6,4))
plt.plot(delta_U - delta_U[0], label='ΔU (kinetische energie, gecentreerd)')
plt.plot(delta_QW - delta_QW[0], '--', label='Q - W (gecentreerd)')
plt.xlabel('Tijdstap')
plt.ylabel('Energie')
plt.legend()
plt.title('Eerste hoofdwet (offset gecorrigeerd)')
plt.show()0
500
1000
1500
2000
2500
3000
3500
4000
4500
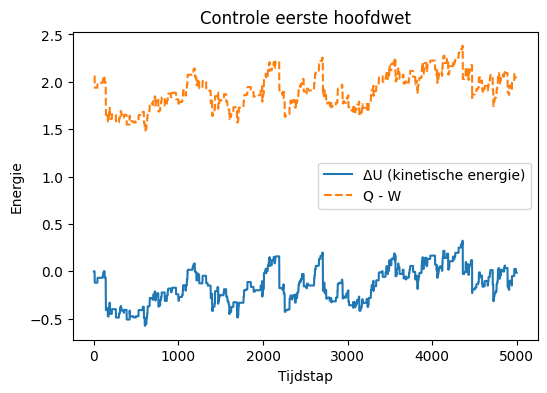
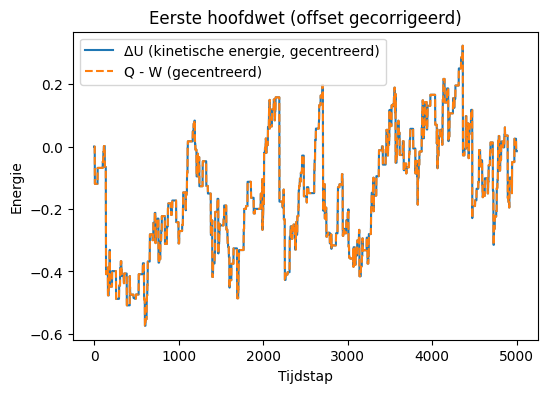
In het boek wordt uitgelegd dat er maar twee vormen van energieoverdracht zijn van een systeem naar de omgeving. Dit kan via warmteoverdracht of via arbeid. Bijzonder is dat deze beide grootheden alleen de snelheid van de moleculen beïnvloeden. Toch zullen we in het volgende werkblad zien dat er een fundamenteel verschil zit in de werking van deze twee macroscopische grootheden.